Há mais de um século, um zoólogo russo, observando ao microscópio larvas transparentes de estrelas-do-mar, lançou as bases da imunologia moderna. Na década de 1880, Ilya Ilyich Metchnikoff observou células móveis a deslocarem-se rapidamente para rodear pequenos espinhos de citrinos que tinha introduzido no corpo das larvas. A partir destas experiências simples emergiu uma ideia radical: certos glóbulos brancos engolem e destroem ativamente agentes nocivos — um processo a que chamou fagocitose.
Na época, a proposta de Metchnikoff de que a inflamação era um mecanismo protetor, e não patológico, foi recebida com ceticismo por figuras de referência como Louis Pasteur e Emil von Behring. A história, porém, viria a dar-lhe razão. Metchnikoff recebeu o Prémio Nobel em 1908, e hoje a fagocitose é um pilar central da imunologia.
Mais de cem anos depois, um novo trabalho liderado pelos investigadores do GIMM Rui Martins e Birte Blankenhaus, do laboratório de Miguel Soares, expande a visão original de Metchnikoff. O estudo, publicado no The EMBO Journal (Homeostatic control of energy metabolism by monocyte-derived macrophages), revela que os macrófagos fazem muito mais do que defender o organismo contra infeções. Funcionam como guardiões metabólicos, capazes de detetar stress sistémico, reciclar componentes celulares danificados e sustentar a função de órgãos inteiros quando processos metabólicos fundamentais falham — mantendo, por exemplo, o coração a bater em situações em que, de outra forma, os ratinhos morreriam após a disrupção da homeostase do ferro.
Dez anos para revelar um sistema de resgate invisível
Os resultados são fruto de quase uma década de investigação, envolvendo dezenas de modelos animais e uma extensa série de experiências tecnicamente exigentes. O desfecho é o estudo de 45 páginas, agora publicado no The EMBO Journal, que revela um mecanismo até aqui desconhecido que liga o metabolismo do ferro, a saúde mitocondrial e o equilíbrio energético do organismo como um todo.
“Este foi um projeto muito longo, com muitas camadas experimentais, porque queríamos ter absoluta certeza de que aquilo que estávamos a observar era real e robusto”, explica Rui Martins, primeiro autor do estudo. “Só os transplantes de medula óssea [realizados ao longo do trabalho] demoram meses a completar e têm de ser feitos em paralelo em múltiplos modelos.”
A vida multicelular depende de uma comunicação constante entre órgãos para manter parâmetros vitais como a produção de energia, a temperatura corporal e o equilíbrio de nutrientes. Quando esta rede é interrompida, as consequências são frequentemente catastróficas. O novo estudo mostra que, quando o metabolismo do ferro colapsa, os macrófagos assumem o papel de coordenadores centrais de um mecanismo de resgate sistémico.
Ferro: essencial, reativo e indispensável
O ferro está no centro desta história. É um cofator essencial para inúmeras reações metabólicas, em particular nas mitocôndrias, as centrais energéticas da célula, onde sustenta a cadeia de transporte de eletrões e a produção de ATP, a principal molécula energética.
“O ferro está envolvido num número extraordinário de processos metabólicos”, afirma Rui Martins. “Mas é também extremamente reativo. Se estivesse livre no interior da célula, catalisaria reações oxidativas altamente destrutivas.”
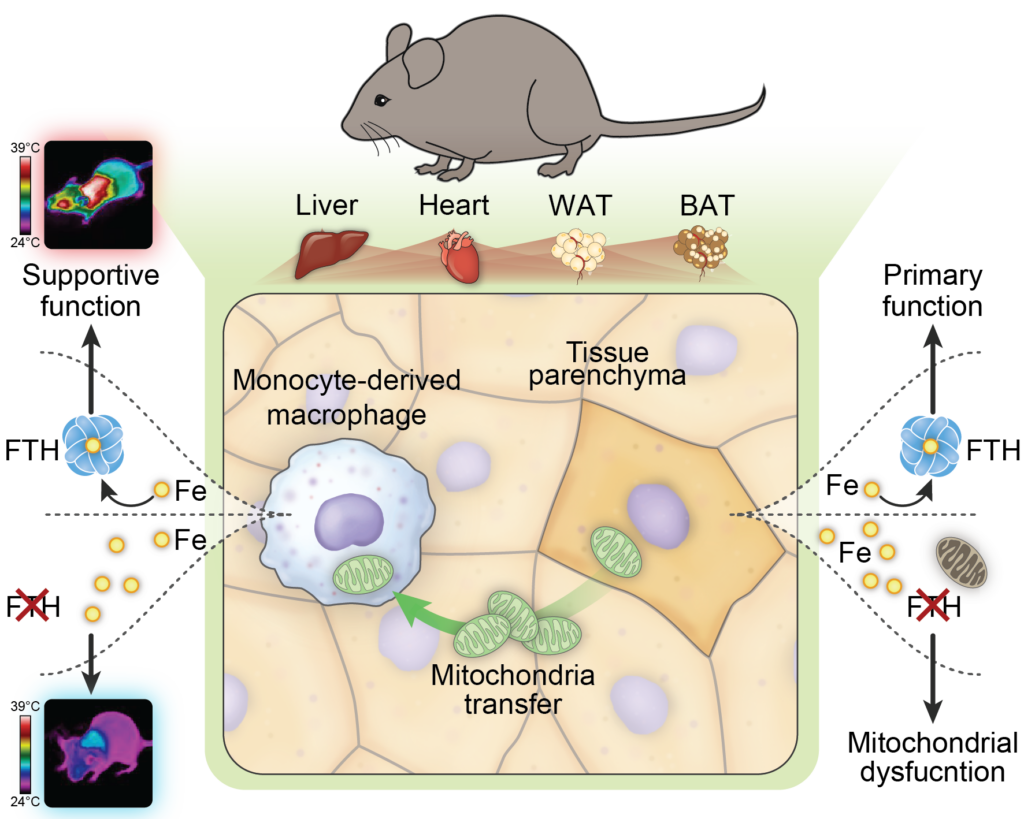
Para gerir este risco, as células controlam rigorosamente o ferro através da ferritina, um complexo proteico que armazena o metal de forma segura. Neste estudo, os investigadores eliminaram geneticamente a cadeia pesada da ferritina (FTH) em tecidos de ratinho, criando uma disrupção controlada do armazenamento de ferro em todo o organismo.
O resultado, já descrito em trabalhos anteriores, foi um colapso metabólico profundo. Apesar de o ferro estar presente, as células não conseguiam utilizá-lo de forma segura ou eficiente — um estado que os investigadores descrevem como uma “falsa deficiência de ferro”. Os animais desenvolveram mitocôndrias disfuncionais, atrofia do tecido adiposo, alterações cardíacas, termogénese comprometida e, por fim, falência multiorgânica e morte.
Posteriormente, os investigadores transplantaram células da medula óssea que expressavam FTH para ratinhos que não expressavam esta proteína — e, surpreendentemente, os animais sobreviveram. Pelo contrário, quando transplantaram medula óssea em que apenas a linhagem de macrófagos não expressava FTH, os ratinhos deixaram de ser resgatados. Estes resultados implicam diretamente os macrófagos no resgate do colapso metabólico e da morte.
“Isto diz-nos que, embora a ferritina seja essencial para a sobrevivência, basta que os macrófagos a expressem para que o organismo inteiro funcione”, explica Martins. “Os tecidos podem ser completamente incapazes de produzir ferritina e, ainda assim, o animal sobrevive.”
O estudo reforça a ideia de que os macrófagos derivados de monócitos atuam como sensores de desequilíbrios do ferro, detetando stress metabólico nos tecidos e desencadeando uma resposta coordenada que previne a falência dos órgãos. Os investigadores descrevem este papel como o de um “ferrostat” celular — um regulador que liga o metabolismo do ferro ao equilíbrio energético à escala do organismo.
Transmitofagia: gestão do lixo mitocondrial à escala do organismo
Nos tecidos que não produzem ferritina, as mitocôndrias acumulam danos oxidativos e tornam-se disfuncionais. Normalmente, as células eliminariam estes resíduos através de um processo de limpeza chamado mitofagia, que é energeticamente exigente. Contudo, em condições de stress metabólico severo, essa capacidade entra em colapso.
O que o estudo demonstra é que as células sob stress exportam as suas mitocôndrias danificadas para os macrófagos, que as englobam e degradam em compartimentos lisossomais — um processo designado por ‘transmitofagia’.
“É quase como um sistema de gestão de resíduos à escala do organismo”, explica Martins. “As células externalizam a eliminação de mitocôndrias danificadas para os macrófagos, que estão melhor equipados para lidar com a carga de ferro e o stress oxidativo.”
Curiosamente, este resultado contrariou a hipótese inicial da equipa. “Pensávamos que os macrófagos poderiam estar a doar mitocôndrias saudáveis aos tecidos”, refere. “Os dados mostraram o oposto — o fluxo é sobretudo das células em stress para os macrófagos.”
Lidar com este influxo mitocondrial exige que os próprios macrófagos sejam metabolicamente robustos. O estudo mostra que a expressão de FTH ativa um programa transcricional controlado pelo TFAM (Mitochondrial Transcription Factor A), um regulador chave da manutenção e biogénese do DNA mitocondrial.
Quando o TFAM foi eliminado especificamente nos macrófagos, o efeito de resgate desapareceu — mesmo na presença de ferritina. Este resultado demonstra que a saúde mitocondrial dos macrófagos é essencial para sustentar o resgate metabólico do organismo.
Para além do ferro: implicações para a doença e a fisiologia
Embora o modelo experimental se baseie numa disrupção artificial do metabolismo do ferro, os autores acreditam que revela um princípio biológico muito mais amplo. Mecanismos semelhantes de remoção mitocondrial mediada por macrófagos já foram descritos no coração, onde a sua falha conduz a doença cardíaca mesmo na ausência de defeitos no metabolismo do ferro.
Esta versatilidade levanta também questões complexas. No cancro, por exemplo, as células tumorais enfrentam stress metabólico intenso. “O que impede uma célula cancerígena de pedir ajuda a um macrófago?”, questiona Martins. Ao apoiar tecidos em sofrimento, os macrófagos podem, em determinados contextos, contribuir inadvertidamente para a progressão da doença.
Vista numa perspetiva histórica, esta descoberta representa uma extensão conceptual direta da intuição original de Metchnikoff. A fagocitose já não é apenas um mecanismo de defesa contra microrganismos; é parte de um sistema sofisticado de manutenção celular, suporte metabólico e resiliência fisiológica.
“Este trabalho mostra que os macrófagos estão na intersecção entre imunidade, metabolismo e comunicação entre órgãos”, conclui Martins. “São verdadeiros canivetes suíços da biologia — adaptáveis, versáteis e indispensáveis para a vida.”